WHO国药三期临床报告第一次曝光,老年人保护率“数据不足”?

药剂博士Calvin.J.Pharm.D
现居加州的药理药剂学博士,原就读于上海医科大学临床医师系,新冠疫情开始以来,他通过油管频道和公益讲座给中国海内外华人做了很多防疫和疫苗的科普。
这几天,WHO的免疫战略咨询专家组(SAGE)完成了对国药评估后批准了国药集团BBIBP-CorV灭活疫苗的紧急使用,得知了这个消息人们在欣喜之余也有些困惑:国药一直都没有公布完整的三期临床的数据,不知道保护率和安全性具体表现如何。
为我们“疫苗护照专栏”提供专业数据参考的江博士在上周WHO国药和科兴三期临床信息汇总解读视频里就预测过国药和科兴很可能获批,我们整理了江博士的上周“原报告解读”视频,希望对想要了解中国国药的朋友们有所帮助。
大家好,今天我要说的是中国国药。
国药从面世以来,除了仅有一个数据显示它的有效率是79%和对重症的保护率是100%之外,基本上没有什么临床数据,直到现在。
因为他们把数据提交给了世卫组织,世界卫生组织对于他们的资料进行汇总,用 PPT的形式向全世界公布。
今天我把英文版的世界卫生组织的国药疫苗的一些数据告诉大家,其实是三期临床的汇总。

| 图 | 我们所说的国药就是中国医药集团(Sinopharm),文中提及为北京生物版本BBIBP。 |
虽然我没有看到三期临床的原版,但是我相信世界卫生组织的医学家们比我更加专业,我在这儿帮大家解读一下这份文件。
对原报告感兴趣的读者可以查看以下下完整16页的PPT文件,链接如下:https://cdn.who.int/media/docs/default-source/immunization/sage/2021/april/2_sage29apr2021_critical-evidence_sinopharm.pdf

对于以上问题由WHO的免疫战略咨询专家组(SAGE)进行分析研究,人员名字都用红色标记(下图),他们算是世界流传病届的大咖级人物。

1.这些数据的来源人数是多少?
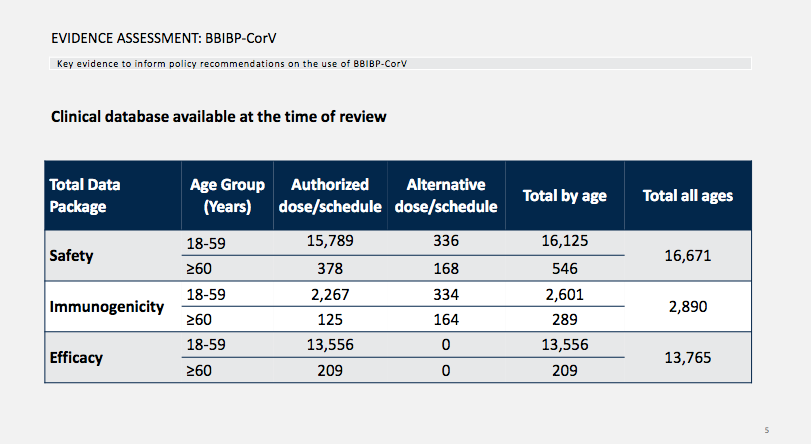
第一个是安全数据,就是说疫苗对比的数据,以上表格显示18~59岁的人一共有15,789人,另有336人用的剂量有些不一样,总人数是16125人;60岁以上的一共有546人。所以加在一起是16,671人。 这里所指的人数是打疫苗组的而不是对照组,所以如果疫苗组和对照组加在一起的话,大概应该有33,000人,基本上和辉瑞(4万左右)、摩德纳(4万左右)、强生(3万多)的人数都差不多。
第二个是查抗体反应提取中和抗体浓度,在18~59岁的人一共有2267人,不同剂量的有334人,合计2601人;60岁以上的共计289人,所以总数是2890人。 因为它只是抗体的浓度,所以它的人数不需要这么多,一般在临床的二期就应该做了。
第三是有效性,一共用了13,765人。 在人数上我认为基本上没有多大问题。
2.这几个临床测试在什么地方做的?
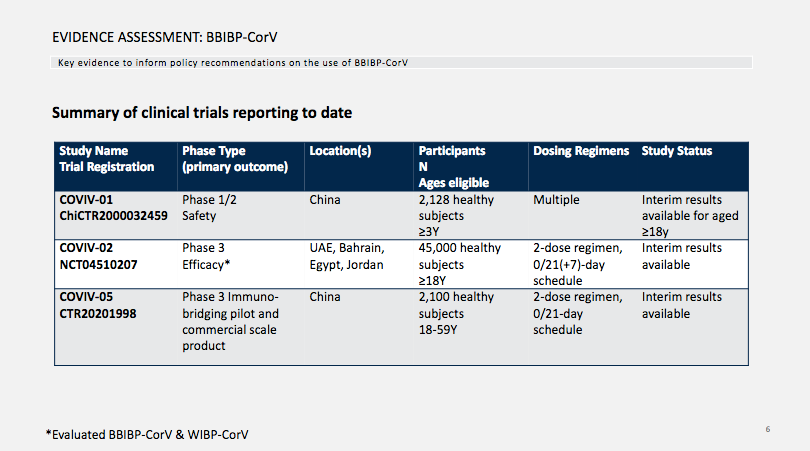
一期二期临床就安全性方面,在我国不同的地区进行,一共是2128人。 因为中国的防疫做得比较好,三期临床只能在外国做的,在阿联酋、巴林、埃及等地做了一共是用了45,000多人,后期又在中国做了一次,是2100多人,大致人数具体在什么地方做的测试,表格都有清楚地呈现。
3.对比在不同的国家加在一起的有效率是多少?
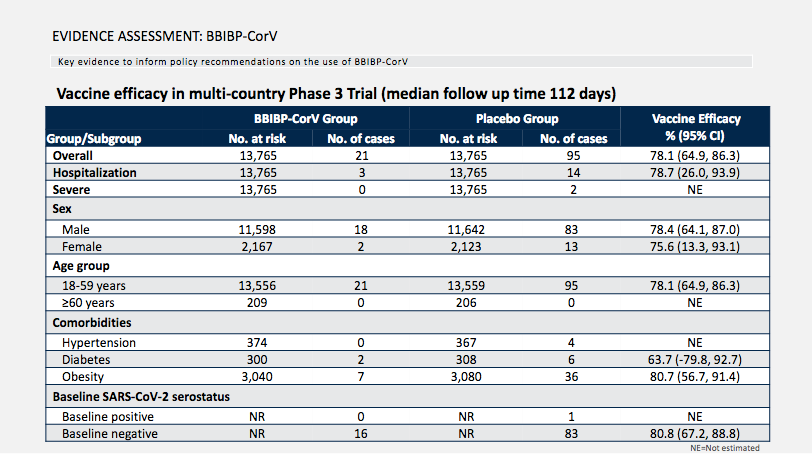
总的有效率:打疫苗的13,765人,在这段时间里面有21人被感染,而在对照组是13,765人有95人被感染,那么总的百分比是78.1%。 但是临床测试它有一个幅度,就是说虽然得到这个数值,但有可能偏低或偏高。 👇为什么?
因为几万人和几亿人,这不是一个概念,所以到了现实生活当中误差还是存在的,其实这个误差的比例应该是64.9%~86.3%。
👇住院人数是怎么回事? 在同样的人数基础上,疫苗组被感染的21人有3人需要住院治疗;而对照组被感染的95人里面有14个人需要住院治疗。
那么之前说对重症的有效率是78.7%,但因为住院的人数少,它这个重症范围又拉大了,基本上从26.0%~93.9%都有可能。
国药刚开始说他们对重症的保护率是100%的时候,我估计他们没有把数据全部归拢就发布消息了,所以说现在来看国药对重症的防治率也不是100%。
👇接近死亡的重症有效率目前无法计算 因为在疫苗组里死亡的重症一个人都没有,对照组里面只有两例,这个数据太小了,世卫组织根本就不能得出结论。
👇不同性别的保护率 男性的有效率是78.4%,女性的有效率是75.6%,但是这个里面有一个很大的问题,男性有11,598人,女性只有2167人,女性的比例太小,所以说这个测试中对女性的保护率无法得出一个非常好的结论,报告呈现女性的保护率是13.3%~93.1%,由此可见一斑。 这个和测试的地方有关,因为测试点很多地方是中东地区,那些国家女性的地位不高,且有各种各样的限制,宗教和习惯的困难造成很难收集到女性的数据,这也是国药走出国门做三期临床所遇到的困难之一。
👇不同年龄段的保护率? 同样数据不足。 涉及年龄组:18~59岁,有13,556人,得到百分比是78.1%;老人60岁以上,疫苗组只有209人,对照组只有206人,疫苗组和测试组两方面都没有案例,所以根本就无法测试对老人是否有效。 然后再看疾病,高血压也是无法计算出来,糖尿病63.7%,肥胖有效率是80.7%。高血压和糖尿病的人数相对来说比较少(300来人),所以说得出的结论相差幅度实在太大,根本就无法得出结论,这是这个实验的缺陷和遗憾。
4.安全性方面得出怎样的结论?

总体来说副作用方面是没有多大问题。一般的情况下都是普通的反应,像头疼劳累,注射地方的疼痛,诸如此类的问题。
疫苗组和对照组两边基本上没有特殊的情况出现,有两例比较重的案例:是打了疫苗后的得了脊髓炎;另一例死亡,但是这一例死亡是在对照组,而不是在疫苗组。
疫苗组的13000多人里面有一例出现血栓现象,从整个安全的数据上看没有过度的危险性,也没有显示特别安全,基本上和辉瑞和摩德纳差不多。
然后在中国在疫苗安全性上又补充一些数据,在整个中国从2020年12月30日到现在已经注射了590万人,其中大概有1453例报告的副作用的的案例。
有补充当然好,但因为不是临床实验这个数据只能做参考,因为临床测试需要接受注射者主动去汇报的话,如果注射者不主动汇报这个数据就有误差,所以这类数据在医学上只能作为一种参考数据,这是世卫组织的观点。

那么对60岁以上的老人,对照组和疫苗组两边都是0,所以它无法得出对老人的保护性到底有多少,但是他们在抗体的研究里面,他们发现60岁以上老人体内的抗体的浓度GMTs和年轻人相比大大降低-“Lower”。不管是中和抗体,还是原其他抗体都降低了。
但也没有看到一些特殊的副作用,79人有45例的副作用,基本上是头晕、头疼、劳累、呕吐、发烧。
发烧量我觉得确实比辉瑞和摩德纳要低很多。头晕反应反而比辉瑞和摩德纳高一点。国药也有过敏反应,就是皮肤过敏像荨麻疹一样的过敏反应也有,这就是我说了它副作用和辉瑞和摩德纳有一点不一样,但是总体来说和普通的疫苗的情况都差不多。
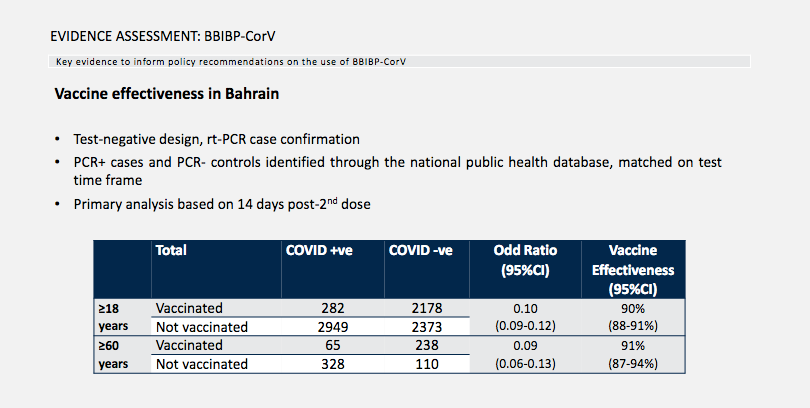
这份报告还补充了巴林的数据,虽然得出91%的数据,但是对于三期临床来说一定要一个大数据,巴林仅有几千人的临床测试,得出的数据只能作为参考。

👇对于基础疾病患者安全性? 因为年轻人的基础疾病人数较少,也基本无法得出结论。 同理,安全性也是一样。

👇对于变异病毒效果到底如何? 对于南非变异病毒B.1.351有效率降低了,但是降低多少,是疫苗无效了,还是具体降低多少无法分析出来,因为数据不全。
5.数据以及资料的缺陷和不足

首先对于严重的重症的保护资料不足,对于变异的病毒资料有点不足,是不是需要加强针也需要多一点数据,对于孕妇、老人的保护数据不足,对于一些后期严重的副作用的数据也是不足。

针对以上短板,国药接下去应该要做的是: 继续跟踪和总结临床实验,从比如秘鲁,阿根廷等地把数据归拢来再重新分析,然后在中国或者在其他地方做儿童的安全性的或者有效性的测试,尽量跟踪中国接受疫苗注射者的后期的各种反应。这是世卫组织建议或者说中国国药下一步的计划。 以上就是国药提供的所有的数据,以及世界卫生组织对他们的分析。
【最后:WHO的评估总结表】
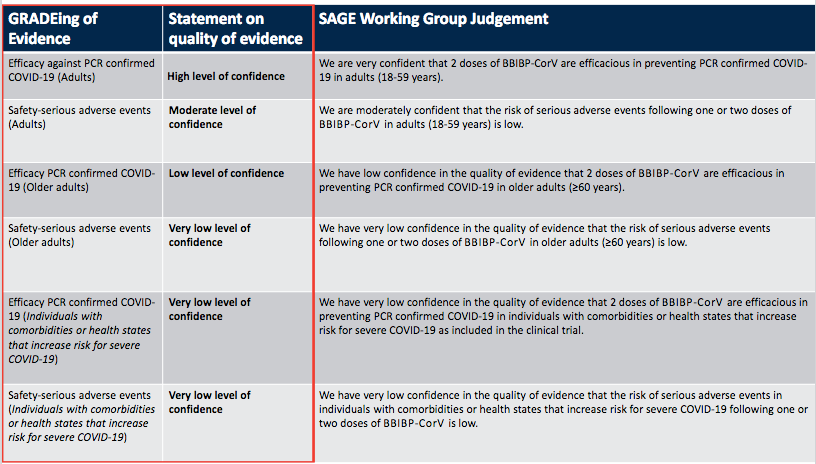
👇对于18岁到59岁的成人的有效性是多少? 对于成人18~59岁人的有效性,我们(SAGE)是较有信心,这个是有效的!
👇那么对于安全性副作用呢? “中等的有效”,刚才说了,数据有些方面跟踪上面后期方面还不是太够完全,WHO 说我们中等感到可以确定没有多大的危险。
👇对于60岁以上的老人的有效性? 我对他们的对疫苗的信心是比较低的,因为数据不足。
👇对于60岁以上的老人的安全性? 对疫苗的信心是很低的,因为数据不足。
👇对于有基础疾病的或者说身体不是太健康人群有效安全? 他们也是说关于“这个疫苗对于这类人是安全的”我们非常低的信心。
特别注意:这些并不是说临床数据显示出,国药疫苗对以上人群是不安全的,主要原因是因为临床的数据不够!

中国疫苗是一个年轻的产业,是中国改革开放以后是慢慢吸收了国外的疫苗的经验和技术开发出来的,发展时间太短,所以在做临床测试上面,他们也没有经验。
另外这次中国的疫情控制得很好,所以只能在其他国家做了三期临床,在很多数据的收集方面以及整理方面,再加上自己没有什么多大的经验,在这个方面很多地方又出现了漏洞和缺陷,是中国疫苗的硬伤。
我希望作为一个起点,将来中国的疫苗的事业或者研发上面能够克服这一系列的不足,能做得更加完美。
从专业的角度来看的话,世界卫生组织由于当前的疫情来说应该会批,但是他批了之后可能会有限制,国药只能用于60岁以内的年轻人,这个可能性比较大,因为他们对老人和基础疾病的人群的数据不够,他们可能加了一些限制在里面,这个是最大的可能性了,当然我有可能是错误的,但是从这个数据上来看,而且从他的语气上来看的话,我觉得这个可能性比较大。 那么我们拭目以待,谢谢大家。
文中所提及的“国药”就是中国医药集团(Sinopharm),其研发的灭活疫苗有两种,分别由旗下北京生物和武汉生物各自研发。北京生物版本BBIBP-CorV五月七日已被世界卫生组织批准紧急使用(EUL),WHO认为BBIBP-CorV易于储藏更适用于低收入国家。需要了解 中国疫苗的分析和对比,点击标题可查看。走啦将在下期整理出江博士就科兴疫苗第三期临床报告解读,敬请关注。









